UNG THƯ TUYẾN TIỀN LIỆT
- Ryan Mark, MD, Sidney Kimmel Cancer Center at Thomas Jefferson University
Ung thư tuyến tiền liệt thường là ung thư biểu mô tuyến. Triệu chứng thường vắng mặt cho đến khi khối u tăng trưởng gây tiểu máu và/hoặc đái khó kèm theo đau. Gợi ý chẩn đoán khi thăm trực tràng hoặc khi xét nghiệm PSA và chẩn đoán xác định bằng sinh thiết qua trực tràng dưới siêu âm. Sàng lọc vẫn là vấn đề gây tranh cãi. Tiên lượng cho hầu hết bệnh nhân ung thư tuyến tiền liệt, đặc biệt ung thư cục bộ hoặc vùng (thường là trước khi có triệu chứng) là rất tốt; nhiều nam giới tử vong do nguyên nhân khác khi đang bị ung thư tiền liệt tuyến hơn là tử vong do bệnh này. Điều trị bằng phẫu thuật cắt tiền liệt tuyến, xạ trị, liệu pháp giảm nhẹ (ví dụ như liệu pháp hormon, xạ trị, hóa trị liệu), hoặc đối với nhiều bệnh nhân lớn tuổi và thậm chí là các đối tượng trẻ chọn lọc, cần giám sát chủ động.
Ung thư tuyến tiền liệt là ung thư phổ biến nhất trong các ung thư không phải ung thư da ở nam giới > 50 tại Mỹ. Tại Mỹ, có khoảng 161.360 trường hợp mới và khoảng 26.730 ca tử vong (ước tính năm 2017) xảy ra mỗi năm (1). Tần suất gia tăng với mỗi thập kỷ; các nghiên cứu tử thi cho thấy ung thư tuyến tiền liệt ở 15-60% nam giới từ 60 đến 90 tuổi, với tỷ lệ mắc tăng theo tuổi. Nguy cơ chẩn đoán mắc bệnh ung thư tuyến tiền liệt trong suốt cuộc đời là 1/6. Tuổi trung bình khi chẩn đoán là 72 và > 75% ung thư tuyến tiền liệt được chẩn đoán ở nam giới > 65. Nguy cơ cao nhất đối với nam giới da đen.
Sarcoma tuyến tiền liệt là rất hiếm, xảy ra chủ yếu ở trẻ em. Ung thư tuyến tiền liệt không biệt hoá , ung thư biểu mô tế bào vảy và ung thư biểu mô ống tuyến chuyển tiếp cũng xảy ra không thường xuyên. Loạn sản nội biểu mô tuyến tiền liệt được coi là một biến đổi mô học tiền ung thư.
Các ảnh hưởng của hormon góp phần vào tiến triển của ung thư biểu mô tuyến tiền liệt, nhưng gần như chắc chắn không ảnh hưởng với các loại ung thư tiền liệt tuyến khác.
Tham khảo chung
- American Cancer Society:Thống kê chính cho ung thư tuyến tiền liệt.
Triệu chứng cơ năng và triệu chứng thực thể
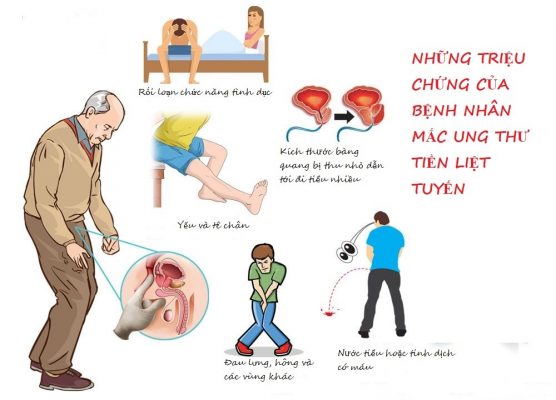
Ung thư tuyến tiền liệt thường tiến triển chậm và hiếm khi gây ra triệu chứng cho đến khi tiến triển. Trong giai đoạn tiến triển bệnh, tiểu máu và các triệu chứng tắc nghẽn bàng quang (ví dụ như bàng quang căng, tiểu ngắt quãng, tia nước tiểu yếu hoặc không liên tục, cảm giác tiểu không hết, tiểu nhỏ giọt cuối bãi) có thể xuất hiện. Đau xương, gãy xương bệnh lý, hoặc ép tủy có thể là kết quả của di căn tế bào tạo xương đến xương (thông thường là xương chậu, xương sườn, xương sống).
Chẩn đoán
- Sàng lọc bằng thăm trực tràng và xét nghiệm PSA
- Đánh giá các bất thường bằng sinh thiết kim qua trực tràng
- Phân loại theo mô học
- Chẩn đoán giai đoạn bằng CT và chụp xương
Đôi khi sờ thấy khối lổn nhổn cứng chắc hoặc các nốt khi thăm trực tràng (DRE), nhưng thường là bình thường; cứng chắc và u cục nghĩ đến ung thư nhưng phải được phân biệt với viêm tuyến tiền liệt hạt, vôi hoá tiền liệt tuyến và các rối loạn tuyến tiền liệt khác. Sự lan rộng của các khối cứng chắc đến các túi tinh và dính tuyến 1 bên gợi ý ung thư tuyến tiền liệt tiến triển tại chỗ. Các ung thư tuyến tiền liệt phát hiện qua DRE có xu hướng lớn và > 50% lan rộng xuyên qua bao.
Chẩn đoán ung thư tiền liệt tuyến đòi hỏi phải có sự xác nhận về mô học, thông thường nhất là sinh thiết kim dưới hướng dẫn của siêu âm qua trực tràng (TRUS), có thể thực hiện trong phòng thủ thuật với gây tê tại chỗ. Các vùng giảm âm có nhiều khả năng là ung thư. Thỉnh thoảng, ung thư tuyến tiền liệt được chẩn đoán ngẫu nhiên từ mẫu mô được lấy ra trong quá trình phẫu thuật u phì đại lành tính tuyến tiền liệt (BPH). MRI đa tham số (Multiparametric MRI) là một cách để xác định bệnh nhân nào cần sinh thiết, nhưng việc sử dụng kỹ thuật này không phổ biến. MRI đa tham số rất hữu ích cho việc theo dõi nam giới có kết quả sinh thiết ban đầu âm tính hoặc theo dõi những người cần giám sát chủ động.
Sàng lọc
Hầu hết ung thư tuyến tiền liệt ngày nay được tìm thấy bằng cách sàng lọc kháng nguyên đặc hiệu tiền liệt tuyến (PSA) huyết thanh (và đôi khi là DRE). Việc sàng lọc thường được thực hiện hàng năm ở nam giới > 50 năm nhưng đôi khi bắt đầu sớm hơn đối với những người có nguy cơ cao (ví dụ những người có tiền sử gia đình mắc bệnh ung thư tuyến tiền liệt và người da đen). Việc kiểm tra thường không được khuyến cáo đối với nam giới có kỳ vọng sống <10 đến 15 tuổi. Các phát hiện bất thường được đánh giá sâu hơn bằng sinh thiết kim dưới siêu âm qua trực tràng.
Tuy nhiên, vẫn chưa rõ liệu sàng lọc có làm giảm tình trạng bệnh tật hoặc tử vong hay không, hoặc có đưa đến bất cứ lợi ích hơn nào từ việc sàng lọc so với sự suy giảm chất lượng cuộc sống do điều trị ung thư không triệu chứng. Việc sàng lọc được khuyến khích bởi một số tổ chức chuyên nghiệp và không khuyến khích ở những tổ chức khác. Một phân tích gần đây của ERSPC (nghiên cứu ngẫu nhiên của châu Âu về sàng lọc ung thư tuyến tiền liệt) và dữ liệu thử nghiệm PLCO (tuyến tiền liệt, phổi, ruột, và buồng trứng) cho thấy rằng việc sàng lọc trong cả hai thử nghiệm chứng minh giảm tỷ lệ tử vong do ung thư tuyến tiền liệt khi kiểm soát sự khác biệt về cường độ sàng lọc mặc dù có tỷ lệ nhiễu cao trong nhánh chứng của PLCO (1,2). Do đó, vào năm 2017, Tổ công tác Dịch vụ Dự phòng Hoa Kỳ đang xem xét lại đề xuất 2012 của họ đối với việc sàng lọc dự phòng hoàn toàn ung thư tuyến tiền liệt (Mức D) với lợi ích có thể (Mức C). Hầu hết các bệnh nhân mới được chẩn đoán ung thư tuyến tiền liệt đều có DRE bình thường và PSA huyết thanh không lý tưởng như một xét nghiệm sàng lọc. Mặc dù PSA tăng từ 25 đến 92% bệnh nhân ung thư tuyến tiền liệt (phụ thuộc vào khối lượng khối u) nhưng nó cũng tăng ở mức độ vừa phải từ 30 đến 50% bệnh nhân bị BPH (phụ thuộc vào kích thước tuyến tiền liệt và mức độ tắc nghẽn) ở một số người hút thuốc, và vài tuần sau khi bị viêm tuyến tiền liệt.
Mức độ≥ 4 ng / mL được xem là chỉ điểm để sinh thiết ở nam giới > 50 tuổi (ở bệnh nhân trẻ tuổi và những người ở tuổi trung niên, > 2,5 ng / ml có thể cho phép sinh thiết vì BPH – nguyên nhân phổ biến nhất gây tăng PSA lại hiếm gặp ở nam giới trẻ tuổi). Mặc dù nồng độ cao là quan trọng (gợi ý tiến triển ngoài vỏ hoặc di căn) và khả năng ung thư tăng lên khi mức PSA tăng, nhưng không có điểm cut-off mà dưới ngưỡng đó bệnh nhân không có nguy cơ.
Ở những bệnh nhân không có triệu chứng, giá trị dự đoán dương tính đối với ung thư là 67% đối với PSA > 10 ng / mL và 25% đối với PSA 4 đến 10 ng / mL; các bằng chứng gần đây cho biết tỷ lệ ung thư ở nam giới ≥ 55 tuổi với PSA < 4 ng / ml là 15% và 10% với PSA giữa 0,6 và 1,0 ng / mL. Tuy nhiên, ung thư có ở nam giới với mức PSA thấp hơn có xu hướng nhỏ hơn (thường là < 1 mL) và độ thấp hơn, mặc dù ung thư độ cao (điểm Gleason 7 đến 10) có thể có mặt ở bất kỳ mức PSA nào; có lẽ 15% trường hợp ung thư biểu hiện với PSA < 4 ng / mL là độ cao. Mặc dù với điểm cut-off 4 ng / ml sẽ lỡ một số bệnh ung thư nghiêm trọng, nhưng chi phí và gánh nặng bệnh tật từ việc tăng số lượng ca sinh thiết để tìm ra bệnh vẫn chưa rõ ràng.
Quyết định có sinh thiết hay không có thể dựa trên các yếu tố liên quan đến PSA khác, ngay cả khi không có tiền sử gia đình mắc bệnh ung thư tuyến tiền liệt. Ví dụ, tốc độ thay đổi PSA (gia tăng PSA ) nên được <0,75 ng / ml / năm (thấp hơn ở bệnh nhân trẻ tuổi). Sinh thiết thường được khuyến cáo với gia tăng PSA> 0,75 ng / mL / năm.
Các xét nghiệm đo tỷ số PSA tự do/toàn phần và phức hợp PSA đặc hiệu với u hơn so với PSA toàn phần chuẩn và có thể làm giảm tần suất sinh thiết ở bệnh nhân không bị ung thư. Ung thư tuyến tiền liệt ít có liên quan đến PSA tự do hơn; không có điểm cut-off chuẩn nào cho PSA tự do, nhưng nói chung, nồng độ < 10 đến 20% hướng đến sinh thiết. Các đồng dạng khác của PSA và các marker mới cho ung thư tuyến tiền liệt đang được nghiên cứu. Không có dạng xét nghiệm về PSA nào trả lời được mối lo ngại về khả năng lạm dụng quá nhiều sinh thiết. Nhiều xét nghiệm mới (ví dụ, kháng nguyên ung thư tuyến tiền liệt tuyến tiền liệt 3 [PCA-3], chỉ số sức khoẻ tuyến tiền liệt PHI, 4Kscore, SelectMDX nước tiểu và những thứ khác) được thương mại hoá và có thể là những trợ giúp hữu ích trong các quyết định sàng lọc.
Các bác sĩ nên thảo luận về những nguy cơ và lợi ích của việc xét nghiệm PSA với bệnh nhân. Một số bệnh nhân muốn loại trừ ung thư bằng mọi giá cho dù khả năng ung thư tiềm tàng và di căn có thể thấp và họ có thể muốn xét nghiệm PSA hàng năm. Những người khác cần chất lượng cuộc sống cao và họ có thể chấp nhận nguy cơ; vì vậy họ xét nghiệm PSA ít thường xuyên hơn (hoặc không xét nghiệm).
Phân độ và giai đoạn
Việc phân độ, dựa trên sự giống nhau của cấu trúc khối u với cấu trúc tuyến bình thường, giúp xác định tính ác tính của khối u. Phân độ dựa vào sự không đồng nhất mô học trong khối u. Điểm số Gleason thường được sử dụng. Mẫu phổ biến nhất và mẫu phổ biến sau đó, mỗi mẫu được chia độ từ 1 đến 5, sau đó cộng điểm độ của hai mẫu vào để tạo ra tổng số điểm. Hầu hết các chuyên gia đều cân nhắc số điểm ≤ 6 là biệt hóa cao, 7 là biệt hóa vừa và 8 đến 10 là kém biệt hóa. Điểm số càng thấp, sự tiến triển và xâm lấn càng ít và tiên lượng càng tốt. Đối với khối u tại chỗ , điểm Gleason giúp dự đoán khả năng xâm lấn vỏ, xâm lấn túi tinh và lan đến các hạch bạch huyết. Gleason độ 1 và 2 hiện không dùng; kết quả là, điểm thấp nhất có thể (3 + 3) là 6. Tuy nhiên, điểm Gleason là 6 không có vẻ thấp khi dùng thang điểm trước đó, từ 2 đến 10. Để giúp truyền đạt điều này cho bệnh nhân, và để đơn giản hóa việc phân loại bệnh lý, một hệ thống tính điểm mới được WHO chấp nhận vào năm 2016, hiện đang được sử dụng:
Nhóm độ 1 = Gleason 3 + 3
Nhóm độ 2 = Gleason 3 + 4
Nhóm độ 3 = Gleason 4 + 3
Nhóm độ 4 = Gleason 8
Nhóm độ 5 = Gleason 9 và 10
Điểm Gleason, giai đoạn lâm sàng và mức độ PSA (sử dụng bảng hoặc toán đồ) kết hợp lại dự đoán giai đoạn bệnh lý và tiên lượng tốt hơn khi dùng chúng một cách đơn lẻ.
Ung thư tuyến tiền liệt phân giai đoạn để xác định mức độ lan rộng khối u (xem Bảng: Phân loại giai đoạn ung thư tuyến tiền liệt AJCC / TNM * và xem Bảng: Định nghĩa TNM đối với ung thư tuyến tiền liệt). Siêu âm qua trực tràng (TRUS) có thể cung cấp thông tin giai đoạn, đặc biệt là sự xâm lấn vỏ và xâm lấn túi tinh. Bệnh nhân có giai đoạn lâm sàng T1c đến T2a, điểm Gleason thấp (≤ 7) và PSA < 10 ng / mL thường không tiến hành thêm các thăm dò giai đoạn trước khi tiến hành điều trị. Xạ hình xương hiếm khi hữu ích cho việc phát hiện các di căn xương (thường là bất thường do chấn thương biến dạng khớp) cho đến khi PSA > 20 ng / mL hoặc trừ khi điểm Gleason cao (tức là, ≥ 8 hoặc [4 +3]). CT (hoặc MRI) vùng bụng và vùng chậu thường được thực hiện để đánh giá các hạch chậu và hạch sau phúc mạc nếu điểm Gleason từ 8 đến 10 và PSA > 10 ng / mL hoặc nếu PSA > 20 ng / mL với bất kỳ điểm Gleason nào. Hạch bạch huyết nghi ngờ có thể được đánh giá thêm bằng cách sử dụng sinh thiết kim. Chụp MRI với cuộn từ (coil) đặt trong trực tràng cũng có thể giúp xác định xâm lấn tại chỗ của khối u ở những bệnh nhân ung thư tiền liệt tuyến tiền tiến triển cục bộ (giai đoạn T3). Vai trò của xạ hình bằng chất In-111 capromab pendetide để xác định giai đoạn bệnh đang được mở rộng nhưng chắc chắn là không cần thiết cho bệnh giai đoạn sớm, khu trú.
Tăng acid phosphatase huyết thanh – đặc biệt là xét nghiệm enzym – tương quan tốt với sự hiện diện di căn, đặc biệt là ở các hạch bạch huyết. Tuy nhiên, enzym này cũng có thể tăng cao trong BPH (và hơi cao sau khi kích thích mạnh tuyến tiền liệt), đa u tủy xương, Bệnh Gaucher, và bệnh thiếu máu tan máu. Nó hiếm khi được sử dụng để hướng dẫn điều trị hoặc theo dõi bệnh nhân sau khi điều trị, đặc biệt là vì giá trị của nó khi thực hiện bởi phương pháp miễn dịch phóng xạ (phương pháp thường dùng) chưa được xác định. Các xét nghiệm PCR phiên mã ngược đối với các tế bào ung thư tiền liệt tuyến lưu hành đang được nghiên cứu thành các công cụ phân giai đoạn và tiên lượng.
Nguy cơ di căn ung thư thấp nếu
- Giai đoạn ≤ T2a
- Điểm Gleason ≤ 6
- Mức PSA ≤ 10 ng / mL
Khối u T2b, điểm Gleason 7, hoặc PSA > 10 ng / mL được coi là nguy cơ trung bình bởi hầu hết các chuyên gia. Khối u T2c, điểm Gleason ≥ 8 hoặc PSA > 20 ng / mL (hoặc 2 yếu tố nguy cơ trung gian) nói chung có nguy cơ cao.
Nguy cơ di căn ung thư có thể được ước tính theo giai đoạn khối u, điểm Gleason và mức PSA:
- Nguy cơ thấp: Giai đoạn ≤ T2a, điểm Gleason ≤ 6, và mức PSA ≤ 10 ng / mL
- Nguy cơ trung bình: Giai đoạn T2b, điểm Gleason = 7, hoặc mức PSA ≥ 10 và ≤ 20 ng / mL
- Nguy cơ cao: Giai đoạn ≥ T2c, điểm Gleason ≥ 8, hoặc PSA ≥ 20 ng / mL
Cả acid phosphatase và PSA giảm sau khi điều trị và tăng lên khi tái phát, nhưng PSA là dấu hiệu nhạy nhất để theo dõi sự tiến triển của ung thư và đáp ứng với điều trị và gần như đã thay thế acid phosphatase khi tiến hành với mục đích này.
Tham khảo chẩn đoán
- European Randomized Study of Screening for Prostate Cancer.
- Shoag JE:Reevaluating PSA testing rates in the PLCO trial. N Engl J Med 374:1795-1796, May 5, 2016. DOI: 10.1056/NEJMc1515131.
Tiên lượng
Tiên lượng cho hầu hết các bệnh nhân ung thư tuyến tiền liệt là rất tốt, đặc biệt là khi ung thư tại chỗ hoặc ung thư khu trú. Tuổi thọ của những nam giới cao tuổi bị ung thư tuyến tiền liệt có thể khác một chút so với nam giới cùng tuổi mà không bị ung thư, sự khác biệt phụ thuộc vào tuổi và bệnh mắc kèm. Đối với nhiều bệnh nhân có thể kiểm soát sự di căn trong thời gian dài hoặc thậm chí chữa khỏi. Khả năng chữa khỏi, ngay cả khi ung thư có biểu hiện tại chỗ trên lâm sàng, phụ thuộc vào độ và giai đoạn của khối u. Nếu không được điều trị sớm, những bệnh nhân ung thư độ cao, kém biệt hóa có tiên lượng xấu. Ung thư tuyến tiền liệt không biệt hóa, ung thư biểu mô tế bào vảy và ung thư biểu mô ống chuyển tiếp đáp ứng kém với các liệu pháp thông thường. Ung thư di căn không có cách chữa trị. Tuổi thọ trung bình khi bệnh di căn là 1 đến 3 năm, mặc dù một số bệnh nhân có thể sống thêm nhiều năm.
Điều trị
- Đối với ung thư cục bộ trong tuyến tiền liệt, phẫu thuật hoặc xạ trị
- Đối với ung thư ngoài tuyến tiền liệt, liệu pháp giảm nhẹ với liệu pháp hoóc môn, xạ trị hoặc hóa trị liệu
- Đối với một số nam giới có nguy cơ ung thư thấp, giám sát chủ động mà không cần điều trị
Điều trị dựa theo mức PSA, độ và giai đoạn của khối u, tuổi bệnh nhân, các bệnh đồng mắc và kỳ vọng sống. Mục tiêu của liệu pháp có thể là
- Giám sát chủ động
- Cục bộ (nhằm chữa bệnh)
- Hệ thống (nhằm giảm hoặc hạn chế phạm vi khối u)
Hầu hết bệnh nhân, bất kể độ tuổi nào, đều thích liệu pháp điều trị triệt để nếu ung thư đe doạ đến tính mạng và có thể chữa khỏi. Tuy nhiên, điều trị chỉ là giảm nhẹ chứ không phải là tiệt căn nếu ung thư đã lan ra ngoài tuyến tiền liệt vì khả năng khỏi là không có. Chờ đợi thận trọng có thể được sử dụng cho những nam giới không được hưởng lợi từ liệu pháp tiệt căn (ví dụ, vì tuổi già hoặc có bệnh kèm theo); những bệnh nhân này được điều trị bằng các liệu pháp giảm nhẹ nếu các triệu chứng tiến triển.
Giám sát chủ động
Giám sát chủ động thích hợp cho nhiều bệnh nhân > 70 tuổi không triệu chứng, có nguy cơ thấp, hoặc có thể thậm chí là nguy cơ trung bình, ung thư tuyến tiền liệt tại chỗ hoặc nếu đồng mắc với các bệnh lý hạn chế sự sống; ở những bệnh nhân này, nguy cơ tử vong do các nguyên nhân khác lớn hơn là ung thư tiền liệt tuyến. Cách tiếp cận này đòi hỏi phải khám DRE và xét nghiệm PSA định kỳ và theo dõi các triệu chứng. Ở những nam giới trẻ khỏe mạnh có nguy cơ ung thư thấp, giám sát chủ động cũng đòi hỏi sinh thiết lặp lại định kỳ. Khoảng cách tối ưu giữa các lần sinh thiết chưa được thiết lập, nhưng hầu hết các chuyên gia đồng ý rằng nên ≥ 1 năm, có thể ít thường xuyên hơn nếu kết quả sinh thiết âm tính liên tục. Nếu ung thư tiến triển thì cần phải điều trị. Khoảng 30% bệnh nhân đang trải qua giám sát chủ động cuối cùng cũng cần được điều trị. Ở nam giới cao tuổi, giám sát chủ động cho tỷ lệ sống tương đương với phẫu thuật tiền liệt tuyến; tuy nhiên, những bệnh nhân đã phẫu thuật có nguy cơ về di căn xa và tỷ lệ tử vong đặc hiệu do bệnh thấp hơn đáng kể.
Liệu pháp cục bộ
Liệu pháp cục bộ nhằm chữa khỏi bệnh ung thư tuyến tiền liệt và do đó có thể được gọi là liệu pháp tiệt căn. Cắt bỏ tuyến tiền liệt tiệt căn, xạ trị và liệu pháp áp lạnh là những lựa chọn chính. Tư vấn cẩn thận về những rủi ro và lợi ích của các phương pháp điều trị này và sự cân nhắc các đặc điểm của bệnh nhân (tuổi, sức khoẻ, đặc điểm khối u) rất quan trọng trong quá trình ra quyết định.
Phẫu thuật cắt tiền liệt tuyến tiệt căn (loại bỏ tuyến tiền liệt kèm túi tinh và hạch vùng) có lẽ tốt nhất cho bệnh nhân < 70 tuổi có khối u giới hạn ở tuyến tiền liệt. Phẫu thuật cắt tiền liệt tuyến phù hợp với một số người cao tuổi, dựa trên tuổi thọ, bệnh lý đồng mắc và khả năng chịu được phẫu thuật và gây mê. Cắt bỏ tuyến tiền liệt được thực hiện thông qua một vết mổ ở vùng bụng dưới. Gần đây, một phương pháp phẫu thuật bằng nội soi bằng robot đã được phát triển nhằm giảm thiểu sự mất máu và thời gian nằm viện nhưng không được chứng minh có khả năng thay đổi tỷ lệ bệnh tật hoặc tử vong. Các biến chứng bao gồm tiểu không tự chủ (khoảng 5 đến 10%), xơ cứng cổ bàng quang hoặc chít hẹp niệu đạo (khoảng 7 đến 20%), rối loạn cương dương (khoảng từ 30 đến 100% tùy thuộc vào độ tuổi và chức năng hiện tại), và chấn thương trực tràng (từ 1 đến 2%). Phẫu thuật cắt bỏ tuyến tiền liệt tiệt căn bảo tồn thần kinh giúp giảm khả năng rối loạn chức năng cương dương nhưng không phải lúc nào cũng có thể thực hiện được, tùy thuộc vào giai đoạn và vị trí của khối u.
Liệu pháp áp lạnh (phá huỷ các tế bào ung thư tuyến tiền liệt bằng cách đóng băng với que lạnh, tiếp theo là tan băng) ít được dùng; kết quả lâu dài không rõ. Tác dụng ngoại ý bao gồm tắc nghẽn đường ra bàng quang, tiểu không tự chủ, rối loạn chức năng cương dương, đau hoặc chấn thương trực tràng. Liệu pháp áp lạnh không phải là phương pháp phổ biến được lựa chọn ở Mỹ nhưng có thể được sử dụng nếu xạ trị không thành công.
Xạ trị bằng chùm tia ngoài thường cung cấp 70 Gy trong 7 tuần, nhưng kỹ thuật này đã được thay thế bằng liệu pháp xạ trị 3 chiều và bằng phương pháp xạ trị điều biến cường độ (IMRT), cung cấp liều an toàn đến 80 Gy cho tuyến tiền liệt; số liệu cho thấy tỷ lệ kiểm soát cục bộ cao hơn, đặc biệt đối với những bệnh nhân có nguy cơ cao. Giảm chức năng cương cứng xảy ra ít nhất là 40%. Các phản ứng phụ khác bao gồm viêm trực tràng phóng xạ, viêm bàng quang, tiêu chảy, mệt mỏi, và có thể là hẹp niệu đạo, đặc biệt ở bệnh nhân có tiền sử cắt bỏ tuyến tiền liệt qua niệu đạo. Các kết quả với liệu pháp xạ trị bằng chùm tia ngoài, phẫu thuật cắt tuyến tiền liệt triệt để và giám sát chủ động được so sánh trung bình 10 năm sau khi điều trị ung thư tuyến tiền liệt cục bộ, như đã trình bày trong nghiên cứu ProtecT (1). Các hình thức xạ trị mới như liệu pháp proton là tốn kém hơn, và những lợi ích mà nó đem lại cho các nam giới bị ung thư tuyến tiền liệt chưa được xác định rõ ràng. Xạ trị bằng chùm tia ngoài cũng có vai trò nếu ung thư còn lại sau khi cắt bỏ triệt để tiền liệt tuyến hoặc nếu nồng độ PSA bắt đầu tăng sau phẫu thuật và không có di căn.
Liệu pháp chậm là liệu pháp cấy các hạt phóng xạ vào tuyến tiền liệt qua đáy chậu. Những hạt này phát ra một đợt phóng xạ trong một khoảng thời gian hữu hạn (thường từ 3 đến 6 tháng) và sau đó trơ. Các protocol nghiên cứu đang xem xét liệu cấy ghép chất lượng cao được sử dụng đơn độc hay cùng với xạ trị tia ngoài có tốt hơn ở những bệnh nhân có nguy cơ trung bình hay không Liệu pháp chậm cũng làm giảm chức năng cương cứng, mặc dù sự khởi phát có thể chậm hơn và bệnh nhân có thể đáp ứng tốt hơn các thuốc ức chế phosphodiesterase loại 5 so với những bệnh nhân có đám mạch thần kinh bị cắt hoặc bị tổn thương trong quá trình phẫu thuật. Tiểu nhiều lần, tiểu gấp, và ít gặp hơn là bí tiểu thường rất phổ biến nhưng thường giảm dần theo thời gian. Các tác dụng phụ khác bao gồm tăng nhu động ruột; kích thích trực tràng, chảy máu, hoặc loét; và rò trực tràng-tiền liệt tuyến.
HIFU (siêu âm tập trung cường độ cao) sử dụng năng lượng siêu âm cường độ lớn xuyên qua trực tràng để cắt mô tuyến tiền liệt. Nó đã được sử dụng trong nhiều năm ở châu Âu và Canada và gần đây đã có mặt tại Mỹ. Vai trò của công nghệ này trong quản lý ung thư tuyến tiền liệt đang được phát triển; hiện nay, đây là biện pháp là phù hợp nhất cho điều trị ung thư tuyến tiền liệt tái phát sau xạ trị.
Nếu ung thư tuyến tiền liệt thể khu trú nhưng có nguy cơ cao, cần phải phối hợp nhiều liệu pháp khác nhau (ví dụ như đối với bệnh nhân ung thư tuyến tiền liệt nguy cơ cao được điều trị bằng bức xạ chùm bên ngoài, bổ sung liệu pháp hoóc môn).
Liệu pháp toàn thân
Nếu ung thư đã lan rộng ra ngoài tuyến tiền liệt, chữa khỏi là không thể; điều trị toàn thân nhằm giảm hoặc hạn chế sự mở rộng của khối u.
Bệnh nhân có khối u tiến triển cục bộ hoặc di căn có thể được lợi từ việc thiếu hụt androgen do phẫu thuật cắt bỏ tinh hoàn hai bên hoặc dùng thuốc chủ vận LHRH, như leuprolide, goserelin, triptorelin, histrelin và buserelin, có hoặc không kèm theo xạ trị. Chất đối kháng LHRH (ví dụ, degarelix) cũng có thể làm giảm testosterone , thường nhanh hơn các chất chủ vận LHRH. Các chất chủ vận LHRH và chất đối kháng LHRH thường làm giảm testosterone huyết thanh gần giống như cắt tinh hoàn hai bên. Các thử nghiệm LATITUDE và STAMPEDE (2,3) cho thấy bổ sung abiraterone và prednisone (hoặc prednisolone) vào liệu pháp điều trị chuẩn kéo dài thời gian sống ở những bệnh nhân ung thư tiền liệt tuyến tiền liệt di căn nhạy với hoóc môn. Nếu bệnh nhân có khối u lớn, ung thư di căn nhạy cảm với hoóc môn, thì hóa trị liệu đầu tay bằng docetaxel cũng có thể được xem xét thay vì abiraterone (4).
Tất cả các phương pháp điều trị gây thiếu hụt androgen làm mất ham muốn và rối loạn cương dương và có thể gây ra cảm giác nóng bừng. Các chất chủ vận LHRH có thể làm tăng PSA tạm thời. Một số bệnh nhân được lợi từ việc bổ sung thuốc kháng androgen (ví dụ flutamide, bicalutamide, nilutamide, cyproterone acetate [không có ở Mỹ]) để chẹn androgen toàn phần. Phối hợp các thuốc chẹn androgen thường để chỉ các chất chủ vận LHRH kèm với thuốc kháng androgen, nhưng lợi ích của nó có vẻ không nhiều ưu thế hơn so với các thuốc chủ vận LHRH dùng đơn độc (degarelix hoặc cắt tinh hoàn). Cách tiếp cận khác là chẹn androgen ngắt quãng, nhằm làm chậm sự xuất hiện của ung thư tuyến tiền liệt không phụ thuộc androgen và giúp hạn chế một số tác dụng bất lợi của việc thiếu androgen. Việc chẹn adrogen toàn phần được thực hiện cho đến khi mức PSA giảm (thường là mức không thể phát hiện), sau đó dừng lại. Việc điều trị được bắt đầu lại khi mức PSA tăng lên trên một ngưỡng nhất định, mặc dù ngưỡng lý tưởng chưa được xác định. Các lịch trình tối ưu để điều trị và thời gian điều trị không được xác định và thay đổi rất nhiều ở các bác sĩ.
Thiếu androgen có thể làm giảm đáng kể chất lượng cuộc sống (ví dụ như hình ảnh bản thân, thái độ đối với bệnh ung thư và điều trị, mức năng lượng) và gây loãng xương, thiếu máu và mất khối lượng cơ khi điều trị lâu dài. Estrogen ngoại sinh hiếm khi được sử dụng vì chúng có nguy cơ biến chứng tim mạch và huyết khối tắc mạch.
Liệu pháp hoóc môn có hiệu quả trong ung thư tuyến tiền liệt di căn trong một khoảng thời gian giới hạn. Ung thư tiến triển (được chỉ định bởi mức PSA ngày càng tăng) bất kể testosterone ở mức phù hợp với việc cắt bỏ tinh hoàn (<50 ng / dL) được phân loại là ung thư tiền liệt tuyến tiền liệt kháng sự cắt bỏ tinh hoàn Các phương pháp điều trị kéo dài sự sống sót của bệnh ung thư tiền liệt tuyến tiền liệt kháng sự cắt bỏ tinh hoàn (được xác định từ năm 2010) bao gồm:
- Docetaxel (một loại thuốc hóa trị liệu taxan)
- Sipuleucel-T (một vắc-xin có tác dụng tạo miễn dịch đối với tế bào ung thư tiền liệt tuyến)
- Abiraterone (ngăn chặn sự tổng hợp androgen trong khối u cũng như trong tinh hoàn và tuyến thượng thận)
- Enzalutamide (ngăn chặn sự kết hợp androgens với thụ thể của chúng)
- Cabazitaxel (một loại thuốc hóa trị liệu taxan có thể có hoạt tính trong các khối u kháng với docetaxel)
Một số dữ liệu cho thấy rằng điều trị miễn dịch tự thân sipuleucel-T nên được sử dụng khi có dấu hiệu sớm nhất của ung thư tuyến tiền liệt kháng liệu pháp cắt bỏ tinh hoàn. Nhìn chung, điều trị ung thư tiền liệt tuyến kháng liệu pháp cắt bỏ tinh hoàn đang được thử nghiệm sử dụng sớm hơn. Tuy nhiên, lựa chọn điều trị có thể liên quan đến nhiều yếu tố, và có rất ít dữ liệu có sẵn giúp dự đoán kết quả; do đó khuyến cáo nên giáo dục bệnh nhân và hội chẩn để đưa ra quyết định.
Để giúp điều trị và ngăn ngừa các biến chứng do di căn xương (ví dụ, gãy xương bệnh lý, đau, ép tủy), một chất ức chế tế bào hủy xương (ví dụ, denosumab, acid zoledronic) có thể được sử dụng. Xạ trị bằng chùm tia ngoài được sử dụng để điều trị các đợt di căn xương riêng lẻ. Radium-233, phát ra bức xạ alpha, gần đây được tìm thấy để kéo dài sự sống cũng như ngăn ngừa các biến chứng do di căn xương ở nam giới có ung thư tiền liệt tuyến kháng sự cắt tinh hoàn.
Tài liệu tham khảo
- Hamdy FC, Donovan JL, Lane JA, et al:10-year outcomes after monitoring, surgery, or radiotherapy for localized prostate cancer. N Engl J Med 375:1415-1424, 2016. doi: 10.1056 / NEJMoa1606220.
- Fizazi K, Tran N, Fein L, et al:Abiraterone plus prednisone in metastatic, castration-sensitive prostate cancer. N Engl J Med 377(4):352-360, 2017. doi: 10.1056 / NEJMoa1704174.
- James ND, de Bono JS, Spears MR, et al:Abiraterone for prostate cancer not previously treated with hormone therapy. N Engl J Med 377(4):338-351, 2017. doi: 10.1056 / NEJMoa1702900.
- Sweeney CJ, Chen Y-H, Carducci M, et al: Chemohormonal therapy in metastatic hormone-sensitive prostate cancer. N Engl J Med 373(8):737-746, 2015. doi: 10.1056 / NEJMoa1503747.
Bài viết liên quan
GIẢI PHÁP TOÀN DIỆN CHẨN ĐOÁN VÀ ĐIỀU TRỊ CHỨNG ĐẠI TIỆN MẤT ĐỒNG VẬN (DYSSYNERGIC DEFECATION) VÀ SÓN PHÂN (FECAL INCONTINENCE)
Nếu quý đối tác, bệnh viện đang quan tâm tới giải pháp chẩn đoán và điều trị chứng đại tiện mất đồng vận (dyssynergic defecation) và són phân (fecal incontinence) hãy liên hệ chúng tôi để được tư vấn và hỗ trợ chuyên môn. Chúng tôi cung cấp giải pháp chẩn đoán và điều trị chứng đại tiện mất đồng […]
HOÀN THÀNH CHƯƠNG TRÌNH ĐÀO TẠO CẤP CHỨNG CHỈ (CME) CHUYÊN SÂU VỀ “ĐIỀU TRỊ RỐI LOẠN CƯƠNG DƯƠNG BẰNG SÓNG XUNG KÍCH NGOÀI CƠ THỂ” – BỆNH VIỆN ĐA KHOA NÔNG NGHIỆP
Công ty Vinmed là đơn vị cung cấp giải pháp điều trị Erectile dysfunction (ED) Rối loạn cương dương (RLCD) không chỉ là vấn đề sức khỏe mà còn ảnh hưởng lớn đến tâm lý và chất lượng cuộc sống của nam giới. Khóa học đã tập trung vào kỹ thuật sóng xung kích cường […]
TRẺ HÓA ÂM ĐẠO CÓ ĐÁNG KHÔNG ?
Nếu bạn đang cân nhắc đến việc trẻ hóa âm đạo, bạn có thể đã nghe nói đến EmpowerRF của InMode—một hệ thống đột phá về các phương pháp điều trị tại phòng khám được thiết kế để biến đổi và trẻ hóa cơ quan sinh dục nữ. Với những tuyên bố táo bạo là […]
TĂNG CƯỜNG SỨC KHỎE ÂM ĐẠO VỚI EMPOWER RF
Tăng cường sức khỏe và độ săn chắc của âm đạo với Empower RF. EmpowerRF: Lấy lại sự tự tin và kiểm soát EmpowerRF không chỉ là một thiết bị đơn lẻ. Đây là một hệ thống toàn diện có các công nghệ VTone (kích thích cơ điện), FormaV (năng lượng nhiệt được kiểm soát) […]
HỘI CHỨNG TIẾT NIỆU SINH DỤC CỦA THỜI KỲ MÃN KINH – GSM
Hội chứng sinh dục của thời kỳ mãn kinh (GSM) là một tình trạng mãn tính gây ra các thay đổi ở bộ phận sinh dục và đường tiết niệu ở phụ nữ. Đây thường là kết quả của sự thay đổi nội tiết tố trong thời kỳ mãn kinh, có hoặc không đi kèm […]